A parità di efficienza del motore, l'etanolo emette quindi 4,56 / 3,55 = 1,28 volte più CO2 della benzina per fornire lo stesso lavoro.
In altre parole: etanolo emet, 28% CO2 in aggiunta alla benzina.
E non sono inclusi in questo calcolo per l'etanolo:
- i costi di produzione di CO2 per l'impianto di cereali o zucchero
- i costi di raffinazione della pianta nello zucchero
- i costi della distillazione
- costi energetici di fermentazione (ovvero il CO2 emesso per riscaldare la melassa)
Alcuni richiami alla chimica: zucchero, fermentazione, alcool e CO2 ...
Comporta le seguenti masse atomiche che sono alla base di tutti i calcoli: C = 12 g / mol, O = 16 g / mol, H = 1 g / mol
a) Il caso dell'alcool derivante dalla fermentazione dello zucchero
Lo zucchero usato per fare l'etanolo proviene dalla famiglia di diholosides (saccarosio o maltosio) di formula: C12H22O11 (vedi http://fr.wikipedia.org/wiki/Sucre#Chimie ) ha una massa molare di 342 grammi che, idrolizzando ("guadagna" una molecola di acqua), darà 2 molecole di glucosio o 2 * C6H12O6 con una massa molare di 180 grammi per una massa totale di 360 grammi.
Dettagli del glucosio: http://fr.wikipedia.org/wiki/Glucose
La mole di glucosio fermenterà secondo l'equazione:
Codice: tout sélectionner
C6H12O6 --> 2*C2H6O + 2*CO2Prodotti: moli 2 di alcol etilico (C2H6O = 46g / mol) e due moli di anidride carbonica (= CO2 44g / mol).
Prima di essere bruciato e trascurando ogni altra emissione di CO2, ogni grammo di alcol prodotto rilascerà quindi, durante la sua "creazione": 44/46 = 0.95 grammi di CO2.
E questo PRIMA della sua combustione. Durante la combustione di alcol:
Codice: tout sélectionner
C2H6O + 7/2*O2 --> 2*CO2 + 3*H2O o per coloro che preferiscono numeri tondi:
Codice: tout sélectionner
2*C2H6O + 7*O2 --> 4*CO2 + 6*H20Errore di bilanciamento sui reagenti, rettifica (che non modifica i risultati sul CO2):
Codice: tout sélectionner
C2H6O + 3*O2 --> 2*CO2 + 3*H2O Durante la combustione, questa mole di 46 g di alcol produrrà quindi 88 g di CO2 (moli 2).
Pertanto, si ottiene un totale di moli 3 di CO2 emessi per mole di alcool bruciato: 1 durante la fermentazione e 2 durante la combustione. In totale 3x44 = 132 g di CO2 per 46 grammi di alcol bruciato.
Conclusione: ogni grammo di alcol emette quindi durante la sua elaborazione e combustione almeno 132 / 46 = 2,87 grammi di CO2.
Dico almeno perché molte "posizioni CO2" non sono state prese in considerazione: la produzione di zucchero e la distillazione di alcol sono senza dubbio le più assetate di energia.
Questo valore di 2,87 g CO2 / g di alcol è quindi un valore molto minore!
b) Il caso della benzina (che l'alcol dovrebbe sostituire)
Riprendo senza dettagliare i calcoli di questa pagina: equazioni di combustione e CO2
Emissioni di CO2 per un idrocarburo di formula C2H (2n + 2) = 44n
Applicazione a benzina (puro ottano). n = 8
[C8H18] = 8 12 * + = 18 1 114 * g / mol.
La massa di CO2 rilasciata per mole di ottano consumato è: 44 * 8 = 352 g.
Il rapporto di consumo di carburante sulle versioni di CO2 è 352 / 114 = 3,09
Conclusione: ogni grammo di benzina emette durante la sua combustione 3,09 grammi di CO2
Il costo della "raffinazione" essendo, nel peggiore dei casi, il 15%, si otterrebbero 3.55 g di CO2 per la raffinazione e la combustione della benzina.
c) Confronto dell'energia con etanolo e benzina
Codice: tout sélectionner
PCI ethanol = 26 900 kJ/kg
PCI essence = 42 700 kJ/kg
A velocità del motore, 42,7 / 26,9 = è necessaria più massa di etanolo per fornire la stessa energia, ovvero i tempi 1,59.
In isoenergy, è quindi necessario aggiungere un coefficiente di 1,59 alle emissioni di CO2 di etanolo: i grammi di 2,87 diventano quindi grammi di 4,56. E ricorda: questi 2,87 g erano già in gran parte negativi perché non tenevano conto della cultura dello zucchero (ma gli scettici diranno, a ragione, che per la benzina non abbiamo tenuto conto del costo di estrazione e trasporto di greggio)
Conclusione generale
Per fornire la stessa quantità di energia di combustione, le emissioni di CO2 sono rispettivamente:
- con benzina: 3,55 grammi di CO2
- con etanolo: 4,56 grammi di CO2
A parità di efficienza del motore, l'etanolo emette quindi 4,56 / 3,55 = 1,28 volte più CO2 della benzina per fornire lo stesso lavoro.
In altre parole: etanolo emet, 28% CO2 in aggiunta alla benzina.
E non sono inclusi in questo calcolo per l'etanolo:
- i costi di produzione di CO2 per l'impianto di cereali o zucchero
- i costi di raffinazione della pianta nello zucchero
- i costi della distillazione
- costi energetici di fermentazione (ovvero il CO2 emesso per riscaldare la melassa)
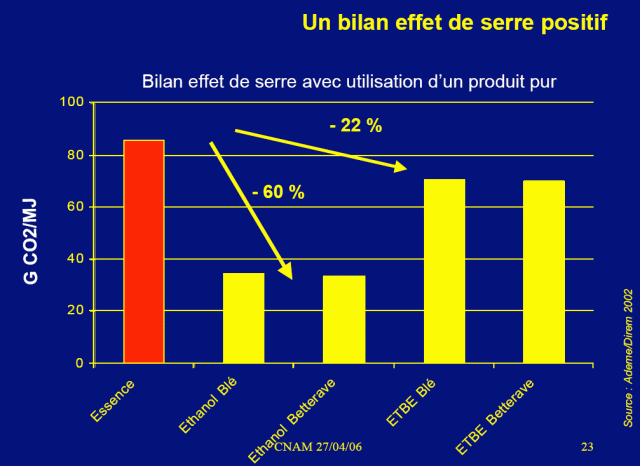
Non vi è quindi alcun dubbio che, sulla base di questo ragionamento, l'etanolo di origine agricola emette molto più CO2 della benzina. Quindi, come possono le agenzie statali e le università ottenere recensioni CO2 sull'etanolo in modo positivo? Non prendono in considerazione la fermentazione? Le omissioni sono? O dov'è il difetto nel nostro ragionamento?